北京市科学技术研究院(以下简称“市科研院”)是北京市人民政府直属的综合性科研机构,地处北京中关村科学城,位于中关村国家自主创新示范区的核心区。作为北京市人民政府直属的综合性科研机构,落实创新驱动发展战略,融入北京(京津冀)国际科技创新中心建设,服务新时代首都高质量发展,肩负重大的职责使命。
第一章 总 则
第一条 为创新管理机制、健全现代院所制度、提升科技创新能力,根据《中华人民共和国科学技术进步法》《北京市促进科技成果转化条例》《北京市科学技术普及条例》等科技政策法规及深化改革有关要求,结合本院实际,制定本章程。
第二条 北京市科学技术研究院是北京市人民政府直属综合性科研机构,成立于1984年,简称市科研院,英文名称为Beijing Academy of Science and Technology(英文缩写BJAST)。市科研院开办资金5000万元,出资人为北京市人民政府。住所为北京市海淀区西三环北路27号,登记机关为北京市事业单位登记管理局。院长为拟任法定代表人的人选,经事业单位登记管理机关依法核准后生效。

《科技智囊》杂志秉持“智囊为魂,科技为体,业界为用,管者必读”的办刊方针,是北京市科学技术研究院主管、主办的新型高端智库期刊。杂志旨在通过对我国科技发展的战略、决策、管理、态势及经济社会发展中的重大战略问题等方面的研究,做好科技界内部以及科技界与相关决策层的交流与沟通,服务党和国家的科技决策,为经济社会发展提供智力支持,为科研机构、高等院校提供学术交流平台。
发布时间:2024年11月08日 14:17
图1.论文发表图
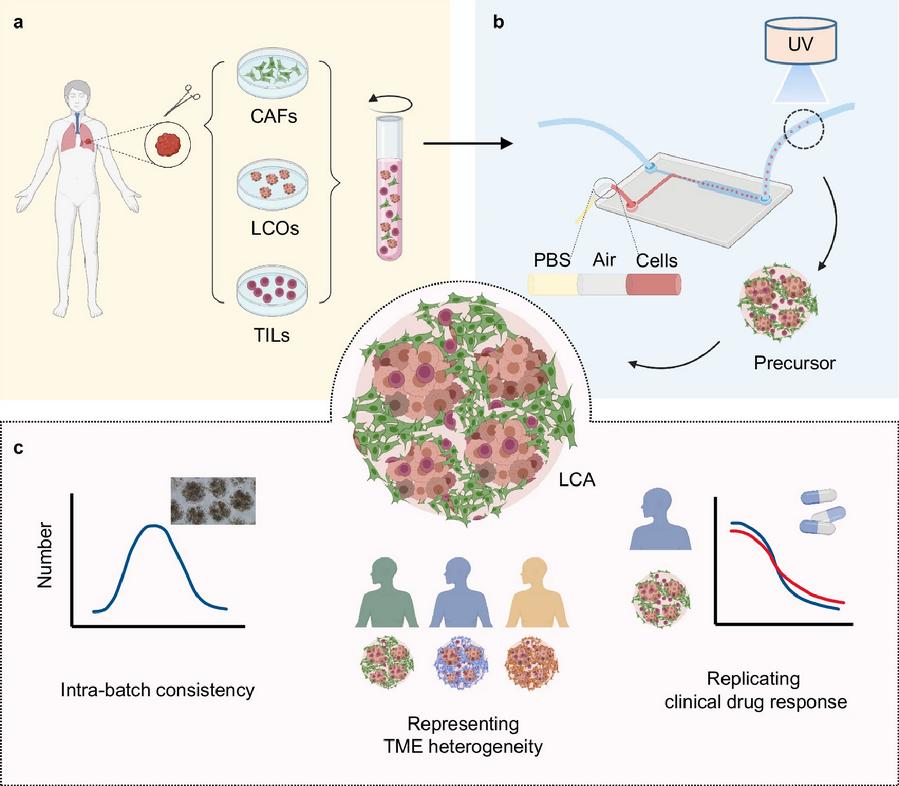
图2. 肺癌类组装体(LCA)模型构建流程及特性
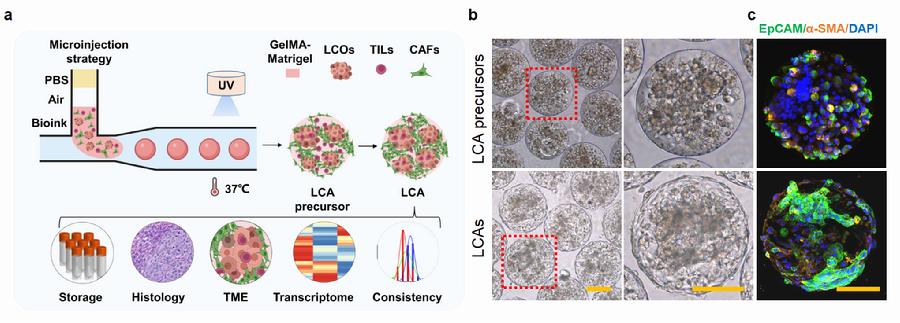
图3. LCA模型制备技术与表征
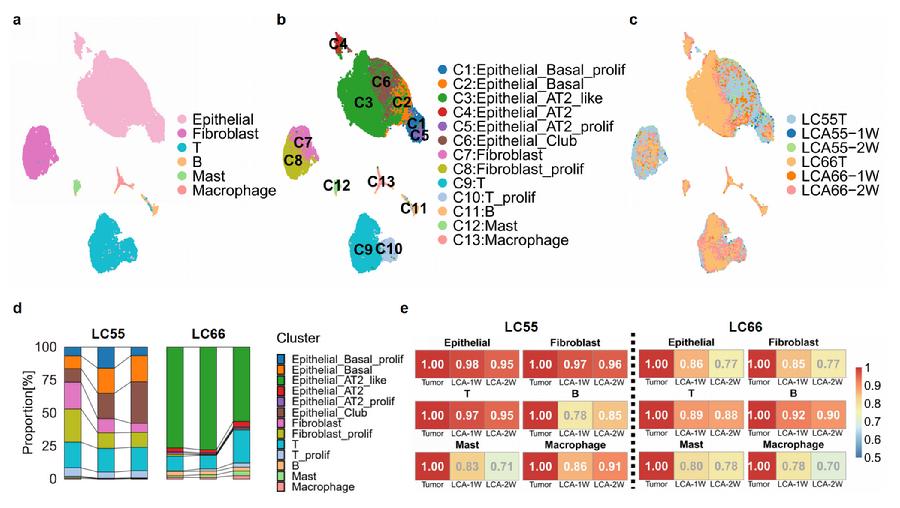
图4. LCA模型具有肿瘤异质性和微环境特征
图5.LCA模型具有良好的临床药物响应一致性
肿瘤模型是肿瘤研究和肿瘤治疗评估的重要工具,也是抗肿瘤药物研发的关键限速因素。如何快速精准构建具有异质性肿瘤微环境的个性化肿瘤模型是肿瘤研究与治疗领域亟待解决的关键问题。肿瘤模型的精准构建是北科院十四五规划的研究内容之一,也是我院前沿技术重点研发方向的主要研究内容之一。
近期,北科院新材料与先进制造研究所生物制造团队合作开发了基于液滴微流控技术快速精准构建个体化肺癌类组装体(lung cancer assembloid, LCA)模型。该LCA模型具有良好的批次内一致性,体外重现了个体化肿瘤的异质性和微环境,可精准预测临床病人药物的响应性,为肿瘤个性化治疗和药物精准筛选提供了一种新模型,具有重要的转化应用前景。该研究成果以题为“A patient-specific lung cancer assembloid model with heterogeneous tumor microenvironments”发表在了Nature子刊Nature Communications(影响因子16.6/Q1,Top)。
传统的肿瘤模型无法重现体内肿瘤的三维结构和复杂微环境,当下热门模型肿瘤类器官存在成分单一,微环境缺乏、批次内一致性差和通量低等问题。为了实现快速精准构建具有肿瘤微环境的LCA模型,研究团队开发了基于微量上样策略的液滴微流控技术和具有良好原代细胞生物相容性的水凝胶材料,并将肺癌患者来源的肺癌类器官、肿瘤相关成纤维细胞(CAFs)和肿瘤浸润淋巴细胞包埋于优化的水凝胶材料中形成大小为400微米左右的类组装前体,体外培养3-5天形成具有类肿瘤组织结构的LCA模型。该技术具有精准微量控制、快速精确成型特征,可以对临床穿刺样本来源的微量细胞进行精准上样控制。另外,LCA模型个体之间具有良好的大小尺寸和细胞分布的一致性。类组装模型可以直接冻存和复苏,并维持很好的类组织结构形态和细胞活性,为LCA模型存储成库奠定基础。
为了充分验证LCA模型的有效性,研究团队通过转录组、基因组、单细胞测序和病理染色分析等方法在分子、细胞和组织层面全方位证明了LCA模型与对应体内肿瘤的相似性,同时发现LCA 模型可以体外重构功能异质的CAFs,体现CAFs对肿瘤药物响应性的影响。这是肿瘤类器官所缺乏的功能。
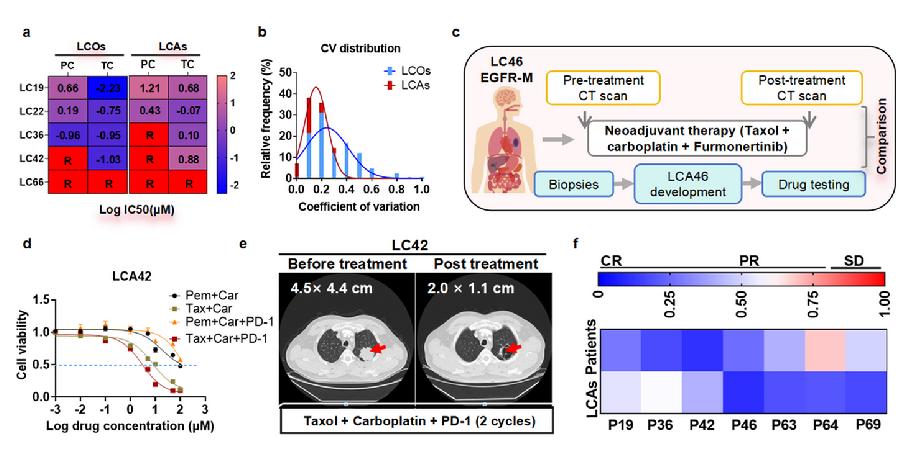
肿瘤模型是否可作为药物精准筛选和个性化诊疗的精准模型,公认的标准包括:1)药物筛选平行组间的一致性和可重复性;2)反应临床药物响应的个体间异质性;3)临床病人药物响应预测的精准性。研究团队分别进行了验证,发现基于LCA模型的药物测试结果可重复性强、平行组间一致性好,而且可以充分反应个体间药物响应的差异性,并且可以很好地预测临床靶向治疗和基于PD-1的免疫联合化疗,7例临床病人的药物响应的预测准确性达到100%。充分证明了LCA模型可以作为理想的肿瘤药物筛选模型和个性化指导用药模型。团队未来将在更多样本和更多癌种中进一步验证模型在个性化指导用药中的应用价值。
本研究由北科院新材料与先进制造研究所与清华大学机械系、北京大学肿瘤医院合作完成。张艳梅博士为论文的第一作者,团队成员张青博士、戴建莉博士、王倩倩博士参与了该研究。
论文链接:https://www.nature.com/articles/s41467-024-47737-z
(张艳梅 文/图)